2.GAIA: MATERIA
MATERIAREN EGOERA FISIKOAKOsa ezazu eskema hau, materiaren egoera bakoitzaren ezaugarriak jarriz, baita pauso bakoitzean tenperaturarekin zer gertatzen den azalduz.
MATERIA, NOLA AGERI DEN
Inguratzen gaituen oro da materia.
Egin itzazu ondoren doazkizun gaiei buruzko laburpenak:
- Teoria zinetikoa eta egoera aldaketa: grafika egin eta interpretatu.
- Aipatu egoera aldaketak zenbait baldintzatan.
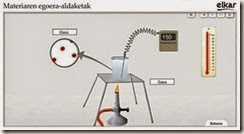
- Ondoren doan link-ean klikatuz gero, Materiaren egera aldaketari buruzko simulazio bat topatu ahal izango duzu. Arretaz egin eta behatu!.
| MATERIAREN EGOERA ALDAKETAK |
GASEN LEGEAK.
XVII. mendetik aurrera zientzilari askok aztertu zuten nolakoa zen gasen portaera presio eta temperatura aldaketen aurrean. Eta hórrela sortu ziren gasen legeak.
Lege horiek eredu zinetiko-molekularraren bidez frogatu ziren eta horrek materiaren egitura korpuskularra ezagutzen lagundu zuen.
Gasak hobekien definitzen dituen propietate fisikoa bolumena da, izan ere, propietate hori presioa eta tenperatura aldatzean erraz aldatzen da. Beraien gainean egindako ikerketek gaurko metodo zientifikoa sortu zuten,eta gasen portaera dagoeneko ezagutzen ditugun legeetan laburbiltzen da:
1.- Boyle-Mariotte-ren legea
Gas baten masa jakin batek betetzen duen bolumena, gasaren presioaren alderantziz proportzionala da, tenperatura konstante mantentzen den artean.
P1·V1=P2·V2=P3·V3=konstante (T konstantean)
Laborategian honako esperientziak egin ditzakegu lege honekin ohartarazteko:
1. esperientzia
Beharrezko materiala:
Beharrezko materiala:
- plastikozko botila handia
- puxika
- flasku garbitzailea
- kristalizadorea
Prozedura:
Kendu iezaiozu tapoia botilari eta jar iezaiozu puxika. Ondo jarrita dagoela konprobatu eta estutu botila. Hau egin eta gero, apurtu ezazu botila erditik eta kristalizadorea edo ontzi handi bat urez beteta dagoela sar ezazu irekita dagoen tokitik, ondo behatuz honek dakarren ondorioa.
Esperimentua egiten duzuen bitartean, atera itzazue argazkiak, eta nahi izanez gero, bideoa ere, geroko laborategi txostena egiteko.
2. esperientzia
Beharrezko materiala:
- plastikozko botila txikia
- CD bat
- lejeda edo kola
- alkohol pixkat bat
- Xaboidun nahaste bat
Prozedura:
Bota ezazu totila barrura alkohol pixkat bat. Botilarena ahoan bota ezazu lekeda eta pegatu CD-a , honen zuloa botilaren zuloaren erdian. Har ezazu atzamarrez xaboidun nahastetik kantitate bat eta estali ondo zuloa. Egin itzazu bi esperientzia, hurrengo legearen frogarako ere balio dezakeena. Lehenengo, estutu botila eta aztertu zer gertatzen den eta bigarrenez, har ezazu botila eskuartean ata saiatu zaitez berotzen. Zer gertatzen da?
Esperimentua egiten duzuen bitartean, atera itzazue argazkiak, eta nahi izanez gero, bideoa ere, geroko laborategi txostena egiteko.
Presio konstantean, gas batek betetzen duen bolumena tenperatura absolutuaren zuzenki proportzionala da.
V1 /T1=V2/T2=V3/T3 =konstante (P konstantean)
Eta laborategian egin dezakegun esperientzia honako hau izan daiteke
Beharrezko materiala:
- Plater bat
- Argizari bat
- Edalontzi bat
- Flasku garbitzailea urarekin
- Txiskeroa
Prozedura
Bota ezazu ur kantitate bat platerraren gainean. Jar ezazu erdian argizaria eta piztu ezazu. Jarraian tapa ezazu edalontziarekin eta behatu ondo gertatzen dena.
Esperimentua egiten duzuen bitartean, atera itzazue argazkiak, eta nahi izanez gero, bideoa ere, geroko laborategi txostena egiteko.
LABORATEGI TXOSTENA
Laborategi txosten batek honako atalak eduki behar ditu:
- Izenburua
- Esperientziaren helburua edo helburuak
- Kontzeptuzko edukinak: zein teoriatan oinarruta dagoen.
- Beharrezko materiala.
- Jarraitutako prozedura.
- Behaketa eta datuen jasoketa.
- Emaitzen analisiak.
- Ondorioak eta iritzi pertsonala.
- Bibliografia.
GASEN LEGEAK APLIKATZEKO ARIKETAK
Hona hemen gasen legeak aplikatzeko buruketa bilduma. Hasteko, adibideak ditugu eta hauek azaldu eta gero, egin itzazu besteak:
Ad: Ontzi batean 0,6m3 gas daude 5 atm-ko presiopean. Kalkulatu gasak zer bolumen izango duen presioa 6 atm-koa demean, tenperatura aldatzen ez bada.
- Datuak:
- Boyle – Mariotte-ren legea aplikatu:
Ariketa: Presio konstatean gertatzen den saiakuntza batean, gasa 285k-ean dago eta 5 L-ko bolumena du. Marraztu, grafiko batean, zer bolumen hartzen duen gasak tenperaturaren funtzioan, 300-400 K tarteko balioetarako.
Orain, buruketa bilduma hemendik deskarga dezakezu:
Presio atmosferikoa
Inprimakiaren amaiera
Lurra inguratzen duen atmosfera gasez osatuta dago eta, gasa materia denez, atmosferak masa du. Atmosferak, guztira, 4 trilioi eta erdi kilogramoko masa duela kalkulatzen da. Baina guri interesatzen zaiguna zera da: masa horrek zenbateko indarra egiten duen, alegia, azalera-unitate bakoitzeko; hau da, zenbatekoa den presio atmosferikoa.
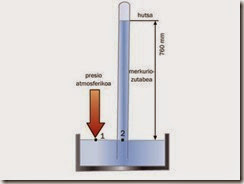
Torricelli izan zen, 1643an, presio atmosferikoa neurtu zuen lehenengoetakoa. Horretarako, ertz bat itxia eta beste irekia zuen beirazko hodi bat merkurioz bete eta, ertz bat irekia zuela, ontzi batean sartu zuen. Hodiak 1,20 m luze neurtzen zuen eta, tututik merkurio apur bat atera arren, hodi barruan beti 760 mm-ko altuera markatzen zuen merkurio-zutabea geratzen zela ikusi zuen. Torricellik ondorioztatu zuen atmosferaren presioak eusten ziola erortzen ez zen merkurioari; hau da, merkurioz betetako ontzian indar bera egiten zutela merkurio zutabeak zein atmosferak. Horregatik, 1 atm eta 760 mm merkurio baliokideak dira.
760 mmHg = 1 atm
Torricelliren esperimentuari jarraituz, Pascalek, 1648an, frogatu zuen, altuerara igotzean, presio atmosferikoa txikiagoa egiten dela. Izan ere, zenbat eta leku altuagoan egon, gaineko gas-zutabea txikiagoa denez, indar gutxiago egiten baitu azalera-unitate bakoitzeko. Nazioarteko SI sisteman presioa neurtzeko erabiltzen den unitateari pascal (Pa) izena eman zaio, zientzialariaren omenez. Pascal bat da newton 1eko indarrak metro koadro 1en egiten duen presioa.
101.325 Pa = 760 mmHg = 1 atm
Presio atmosferikoaren kontzeptua 1654an zabaldu zen jendartera, Magdeburgoko esferaerdien esperimentuari esker.
http://youtu.be/neimvuWI0pU


iruzkinik ez:
Argitaratu iruzkina